Tin tức

Quả hồng vị thuốc tốt cho sức khỏe ngay tại nhà
Hồng là loại trái cây rất phổ biến tại Việt Nam và được nhiều người ưu thích. Quả hồng không đơn giản là thứ quả tráng miệng thơm ngon mà còn là nguồn cung cấp vitamin và chất khoáng dồi dào như
Bệnh

Nước mắt nhân tạo và những lưu ý khi sử dụng
Sở dĩ mắt chúng ta thường có được vẻ long lanh là nhờ lớp nước mắt rất mỏng bao phủ bề mặt nhãn cầu, còn được gọi là phim nước mắt. Nó có vai trò làm sạch mắt, diệt khuẩn, đảm bảo cho giác mạc được
Trẻ em
Viêm tiểu phế quản – Bệnh nguy hiểm cho bé
Viêm tiểu phế quản là một bệnh thường gặp ở trẻ nhỏ nhất là trẻ sinh non. Cần ý thức độ nguy hiểm của bệnh để phòng và điều trị bệnh kịp thời cho trẻ. Viêm tiểu phế quản là gì? Viêm tiểu phế quản
Bà bầu

Những loại thuốc nên tránh khi mang bầu
Bà bầu uống thuốc cần cân nhắc kỹ bởi những ảnh hưởng của thuốc không chỉ tác dụng lên mẹ mà còn lên thai nhi. Dưới đây là 10 loại thuốc nên tránh khi mang bầu. Thuốc giảm đau Thuốc giảm đau như
Sống khỏe

Quả hồng vị thuốc tốt cho sức khỏe ngay tại nhà
Hồng là loại trái cây rất phổ biến tại Việt Nam và được nhiều người ưu thích. Quả hồng không đơn giản là thứ quả tráng miệng thơm ngon mà còn là nguồn cung cấp vitamin và chất khoáng dồi dào như
Sức khỏe phụ Nữ

Cách tính chu kỳ kinh nguyệt có đều hay không?
Kinh nguyệt không đều là những thay đổi về chu kỳ kinh, lúc thu ngắn lại, khi kéo dài ra khiến người phụ nữ không thể dự đoán kỳ kinh tới có thể xảy ra vào ngày nào. Nhiều chị em nghĩ rằng kinh
Sức khỏe Nam giới

Dấu hiệu cảnh báo bạn đang bị viêm tiền liệt tuyến
Tiền liệt tuyến là một tuyến đặc biệt chỉ có ở nam giới, là nơi mà cơ quan sinh dục của nam giới sản xuất ra tinh dịch giúp cho tinh trùng “bơi” trong quá trình xuất tinh. Vị trí của nó nằm bên
Y học quanh ta

Nguyên tắc sử dụng thuốc ở trẻ em
Trẻ em không phải là một người lớn thu nhỏ. Việc sử dụng thuốc cho trẻ cũng không thể chỉ đơn giản là điều chỉnh từ hướng dẫn sử dụng thuốc cho người lớn mà cần có một nguyên tắc riêng biệt, thậm chí
Thuốc và Biệt dược
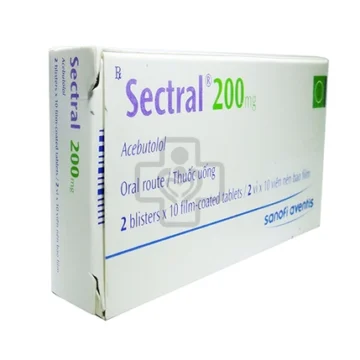
SECTRAL 200
Thuốc Sectral 200 của hãng dược phẩm AVENTIS PHARMA chứa thành phần Acebutolol dạng base có tác dụng điều trị tăng huyết áp, cơn đau thắt ngực. Thành phần thuốc: Viên nén 200 mg: hộp 20