Tin tức

Nghiện rượu mạn tính
Theo WTO, nghiện rượu là sự thèm muốn, đòi hỏi thường xuyên uống rượu, dẫn đến rối loạn nhân cách, giảm khả năng lao động ảnh hưởng đến sức khoẻ con nghiện. Đây cũng là cảnh báo cho những ai đang có
Bệnh
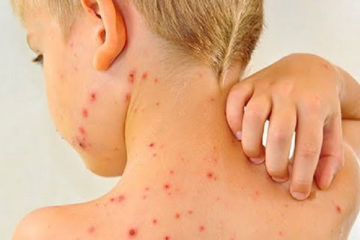
Triệu chứng chân tay miệng ở trẻ em qua từng giai đoạn
Ở nước ta, bệnh chân tay miệng có xu hướng tăng cao vào 2 thời điểm từ tháng 3 - 5 và từ tháng 9 -12. Bệnh thường gặp ở trẻ em nhiều hơn người lớn, bởi trẻ em có hệ miễn dịch yếu. Vậy triệu chứng chân
Trẻ em

Triệu chứng chân tay miệng ở trẻ em qua từng giai đoạn
Ở nước ta, bệnh chân tay miệng có xu hướng tăng cao vào 2 thời điểm từ tháng 3 - 5 và từ tháng 9 -12. Bệnh thường gặp ở trẻ em nhiều hơn người lớn, bởi trẻ em có hệ miễn dịch yếu. Vậy triệu chứng chân
Bà bầu

Làm gì để có thai kỳ khỏe mạnh
Để có thai kỳ khoẻ mạnh, các chuyện gia Trung tâm y học Can-tor, New York (Mỹ) vừa đưa ra một số khuyến cáo về khám các loại bệnh cần thiết trước và trong khi mang thai. Khám răng Trong thời gian
Sống khỏe

Men tiêu hoá cho người lớn nên mua loại nào?
Người trưởng thành là đối tượng có ít thời gian hơn chăm chút cho bữa ăn và sức khỏe của mình. Vì thế vấn đề chướng bụng đầy hơi, rối loạn tiêu hóa thường xảy ra. Men tiêu hóa cho người lớn có phải
Sức khỏe phụ Nữ

Đối tượng dễ mắc bệnh sa sinh dục
Sa sinh dục là một bệnh lý thường gặp ở người lớn tuổi khi các cơ không được khỏe mạnh để nâng đỡ cấu trúc sinh dục như lúc trẻ. Bệnh có thể xảy ra ở cả người nam và nữ, đối với nữ thì đó là chứng sa
Sức khỏe Nam giới

Nghiện rượu mạn tính
Theo WTO, nghiện rượu là sự thèm muốn, đòi hỏi thường xuyên uống rượu, dẫn đến rối loạn nhân cách, giảm khả năng lao động ảnh hưởng đến sức khoẻ con nghiện. Đây cũng là cảnh báo cho những ai đang có
Y học quanh ta

Men tiêu hoá cho người lớn nên mua loại nào?
Người trưởng thành là đối tượng có ít thời gian hơn chăm chút cho bữa ăn và sức khỏe của mình. Vì thế vấn đề chướng bụng đầy hơi, rối loạn tiêu hóa thường xảy ra. Men tiêu hóa cho người lớn có phải
Thuốc và Biệt dược

MORIHEPAMIN – Đạm truyền cho bệnh nhân não gan
Thuốc Morihepamin là một loại thuốc dịch truyền đạm đặc biệt sử dụng trong một số trường hợp cơ thể cần bổ sung các acid amin thiết yếu qua đường tiêm truyền. Thành phần và dạng đóng gói của thuốc