Virus viêm gan C (Hepatitis C virus: HCV) là căn nguyên gây viêm gan. Trên thế giới ước tính 160 – 180 triệu người mắc bệnh. Tỷ lệ nhiễm virus viêm gan C thay đổi tuỳ theo quốc gia, trung bình 0,1% đến 5%.
Mục lục
- 1 1. Phác đồ điều trị viêm gan vi rút C mạn trên người bệnh không xơ gan
- 2 2. Phác đồ điều trị viêm gan vi rút C mạn trên người bệnh xơ gan còn bù
- 3 3. Phác đồ điều trị viêm gan vi rút C mạn trên người bệnh xơ gan mất bù
- 4 4. Theo dõi trong quá trình điều trị viêm gan C mạn tính
- 5 5. Thông tin tham khảo từ BYT Việt Nam
Virus viêm gan C lây truyền qua đường máu (như sử dụng ma tuý, chạy thận nhân tạo chu kỳ), quan hệ tình dục không an toàn với người bị nhiễm bệnh và lây truyền từ mẹ sang con. Nguy cơ lây nhiễm qua tiêm chích ma tuý khoảng 70 đến 90%.
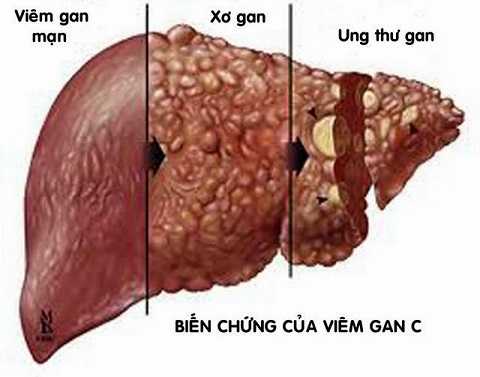
Trước đây phác đồ điều trị viêm gan c mạn hay được dùng nhất tại VN là phác đồ phối hợp 2 thuốc: Peg-Interferon + Ribavirin.
Phác đồ điều trị viêm gan C mạn phải do các bác sĩ chuyên khoa chỉ định vì nó phụ thuộc vào kiểu gen của HCV.
Phác đồ điều trị viêm gan C mạn hiện nay chủ yếu là dùng các loại thuốc uống (DAAs) như: Sofosbuvir, Ledipasvir, Daclatasvir, Elbasvir, Grazoprevir, Velpatasvir …
Phác đồ điều trị viêm gan C mạn dùng các loại thuốc uống (DAAs) có thời gian điều trị trung bình 12 tuần, một số trường hợp cần kéo dài 16-24 tuần.
Phác đồ điều trị viêm gan C mạn bằng DAAs được công nhận và dùng rộng rãi từ năm 2013, nhiều công trình nghiên cứu được công bố cho thấy: Tỷ lệ khỏi bệnh từ 93 – 99%. Các thuốc DAAs phải dùng phối hợp, không được dùng đơn chất. Các phác đồ có DAAs có thể hoặc không phối hợp với Ribavirin.
Ngày 20 tháng 9 năm 2016, Bộ Y Tế đã ký văn bản số 5012/QĐ-BYT ban hành hướng dẫn chẩn đoán, điều trị bệnh viêm gan vi rút C.
Tóm tắt một số phác đồ điều trị viêm gan C mạn (kiểu gen 1, 2 và 6) theo hướng dẫn của Bộ Y Tế Việt Nam.
1. Phác đồ điều trị viêm gan vi rút C mạn trên người bệnh không xơ gan
Phác đồ điều trị viêm gan virus C mạn tính trên người bệnh không có xơ gan tùy thuộc theo Tuýp viêm gan C bị mắc phải.
– Kiểu gen 1 (típ 1)
Sofosbuvir/Ledipasvir thời gian điều trị 12 tuần.
Sofosbuvir + Daclatasvir thời gian điều trị 12 tuần
Elbasvir/Grazoprevir thời gian điều trị 12 tuần
Sofosbuvir/Velpatasvir thời gian điều trị 12 tuần
- Kiểu gen 2 (típ 2)
Sofosbuvir + Daclatasvir thời gian điều trị 12 tuần
Sofosbuvir + Ribavirin thời gian điều trị 12 tuần
Sofosbuvir/Velpatasvir thời gian điều trị 12 tuần
- Kiểu gen 6 (típ 6)
Sofosbuvir/Ledipasvir thời gian điều trị 12 tuần.
Sofosbuvir + Daclatasvir thời gian điều trị 12 tuần
Sofosbuvir/Velpatasvir thời gian điều trị 12 tuần
2. Phác đồ điều trị viêm gan vi rút C mạn trên người bệnh xơ gan còn bù
Phác đồ điều trị viem gan C mạn trên người bệnh xơ gan còn bù theo từng tuýp mắc phải.
Kiểu gen 1 (típ 1)
Sofosbuvir/Ledipasvir thời gian điều trị 24 tuần. (điều trị 12 tuần + Ribavirin)
Sofosbuvir + Daclatasvir thời gian điều trị 24 tuần. (điều trị 12 tuần + Ribavirin)
Elbasvir/Grazoprevir thời gian điều trị 12 tuần
Sofosbuvir/Velpatasvir thời gian điều trị 12 tuần
Kiểu gen 2 (típ 2)
Sofosbuvir + Daclatasvir thời gian điều trị 12 tuần
Sofosbuvir + Ribavirin thời gian điều trị 16 – 20 tuần
Sofosbuvir/Velpatasvir thời gian điều trị 12 tuần
Kiểu gen 6 (típ 6)
Sofosbuvir/Ledipasvir thời gian điều trị 24 tuần. (điều trị 12 tuần + Ribavirin)
Sofosbuvir + Daclatasvir thời gian điều trị 24 tuần. (điều trị 12 tuần + Ribavirin)
Sofosbuvir/Velpatasvir thời gian điều trị 12 tuần
3. Phác đồ điều trị viêm gan vi rút C mạn trên người bệnh xơ gan mất bù
Trên các đối tượng viêm gan C mạn tính ở bệnh nhân xơ gan mất bù, việc điều trị có nhiều khác biệt.
SOF+RBV
SOF/LDV
SOF/DCV
SOF/VEL
Kiểu gen 1,4,5,6
24 tuần hoặc 12 tuần (+RBV)
24 tuần hoặc 12 tuần (+RBV)
24 tuần hoặc 12 tuần (+RBV)
Kiểu gen 2
16-20 tuần
24 tuần hoặc 12 tuần (+RBV)
Kiểu gen 3
24 tuần hoặc 12 tuần (+RBV)
4. Theo dõi trong quá trình điều trị viêm gan C mạn tính
- Lâm sàng: 4 tuần một lần, đánh giá triệu chứng lâm sàng, các tác dụng không mong muốn của thuốc.
- Men gan ALT, tế bào máu ngoại vi, creatinin, mức lọc cầu thận: 4 tuần một lần.
- Đo tải lượng HCV RNA (sử dụng kỹ thuật với ngưỡng phát hiện < 50 IU/ml): tuần 4, 12, 24.
- Tỷ lệ Prothrombin, AFP, siêu âm bụng 12 tuần một lần.
5. Thông tin tham khảo từ BYT Việt Nam
Từ tháng 10/2015 Bộ Y Tế đã cho phép nhập khẩu đơn chất Sofosbuvir và dạng phối hợp Ledipasvir/Sofosbuvirvề Việt Nam để điều trị cho bệnh nhân viêm gan C mạn. Từ tháng 10/2016 Bộ Y Tế đã cho phép nhập khẩu thêm Daclatasvir về Việt Nam.
– Sofosbuvir nhập khẩu có tên thương mại Myhep
– Ledipasvir/Sofosbuvir nhập khẩu có tên thương mại Ledvir.
– Daclatasvir nhập khẩu có tên thương mại Tasvir và NatDac.
Ledvir (Ledipasvir/Sofosbuvir) thuốc được BYT cho phép nhập khẩu về Việt Nam