Mục lục
Avastin là một loại thuốc dùng để điều trị bệnh nhân trưởng thành bị ung thư tiến triển ở ruột già, cũng được sử dụng để điều trị bệnh nhân trưởng thành bị ung thư vú di căn.
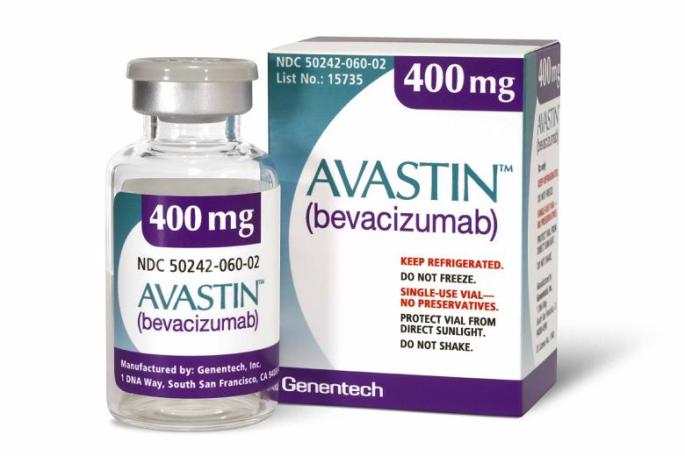
Dạng trình bày và đăng ký thuốc Avastin
Dạng trình bày thuốc Avastin
Chất lỏng trong suốt, không màu đến màu nâu nhạt trong lọ thủy tinh có nút cao su.
Mỗi lọ chứa 100 mg bevacizumab trong 4 ml dung dịch hoặc 400 mg bevacizumab trong 16 ml dung dịch.
Mỗi gói Avastin chứa một lọ.
Dạng đăng kí của thuốc Avastin
Thuốc Avastin đăng ký là thuốc kê đơn – khi sử dụng cần có đơn bác sỹ.
Thành phần của thuốc Avastin
- Các hoạt chất là bevacizumab. Mỗi ml tinh chất chứa 25 mg bevacizumab, tương ứng với 1,4 đến 16,5 mg / ml khi pha loãng theo khuyến cáo.
Mỗi lọ 4 ml chứa 100 mg bevacizumab, tương ứng với 1,4 mg / ml khi pha loãng theo khuyến cáo.
Mỗi lọ 16 ml chứa 400 mg bevacizumab, tương ứng với 16,5 mg / ml khi pha loãng theo khuyến cáo - Các thành phần khác là trehalose dihydrate, natri phosphate, polysorbate 20 và nước để tiêm.
Chỉ định
- Avastin là một loại thuốc dùng để điều trị bệnh nhân trưởng thành bị ung thư tiến triển ở ruột già, tức là ở đại tràng hoặc trực tràng. Avastin sẽ được dùng kết hợp với điều trị hóa trị liệu có chứa thuốc fluoropyrimidine.
- Avastin cũng được sử dụng để điều trị bệnh nhân trưởng thành bị ung thư vú di căn. Khi được sử dụng cho bệnh nhân ung thư vú, nó sẽ được dùng cùng với một sản phẩm thuốc hóa trị liệu có tên là paclitaxel hoặc capecitabine.
- Avastin cũng được sử dụng để điều trị bệnh nhân trưởng thành bị ung thư phổi không phải tế bào nhỏ tiến triển. Avastin sẽ được dùng cùng với chế độ hóa trị liệu có chứa bạch kim.
- Avastin cũng được sử dụng để điều trị bệnh nhân trưởng thành bị ung thư phổi không phải tế bào nhỏ tiến triển khi các tế bào ung thư có đột biến đặc biệt của một protein gọi là thụ thể yếu tố tăng trưởng biểu bì (EGFR). Avastin sẽ được dùng kết hợp với erlotinib.
- Avastin cũng được sử dụng để điều trị bệnh nhân trưởng thành bị ung thư thận tiến triển. Khi được sử dụng cho bệnh nhân ung thư thận, nó sẽ được dùng cùng với một loại thuốc khác gọi là interferon.
- Avastin cũng được sử dụng để điều trị bệnh nhân trưởng thành bị buồng trứng biểu mô tiến triển, ống dẫn trứng hoặc ung thư phúc mạc nguyên phát. Khi được sử dụng cho bệnh nhân bị buồng trứng biểu mô, ống dẫn trứng hoặc ung thư phúc mạc nguyên phát, nó sẽ được dùng kết hợp với carboplatin và paclitaxel.
- Khi được sử dụng cho những bệnh nhân trưởng thành mắc ung thư biểu mô buồng trứng, ống dẫn trứng hoặc ung thư phúc mạc nguyên phát mà bệnh đã quay trở lại ít nhất 6 tháng sau lần cuối họ được điều trị bằng chế độ hóa trị liệu có chứa chất bạch kim, Avastin sẽ được sử dụng kết hợp với carboplatin và gemcitabine hoặc với carboplatin và paclitaxel.
- Khi được sử dụng cho những bệnh nhân trưởng thành bị buồng trứng biểu mô tiến triển, ống dẫn trứng hoặc ung thư phúc mạc nguyên phát mà bệnh đã quay trở lại trước 6 tháng sau lần cuối họ được điều trị bằng chế độ hóa trị liệu có chứa chất bạch kim, Avastin sẽ được sử dụng kết hợp với paclitaxel hoặc topotecan, hoặc doxorubicin pegylated liposome.
- Avastin cũng được sử dụng để điều trị bệnh nhân trưởng thành bị ung thư cổ tử cung dai dẳng, tái phát hoặc di căn. Avastin sẽ được dùng kết hợp với paclitaxel và cisplatin hoặc, thay vào đó, paclitaxel và topotecan ở những bệnh nhân không thể điều trị bằng bạch kim.
Chống chỉ định
Không sử dụng Avastin nếu:
- Bạn bị dị ứng (quá mẫn cảm) với bevacizumab hoặc với bất kỳ thành phần nào khác của thuốc này
- Bạn bị dị ứng (quá mẫn cảm) với các sản phẩm tế bào buồng trứng (CHO) của Trung Quốc hoặc với các kháng thể tái tổ hợp hoặc nhân tạo khác.
- Bạn có thai.
Liều và cách dùng
Liều lượng và tần suất dùng
Liều Avastin cần thiết phụ thuộc vào trọng lượng cơ thể của bạn và loại ung thư cần điều trị. Liều khuyến cáo là 5 mg, 7,5 mg, 10 mg hoặc 15 mg mỗi kg trọng lượng cơ thể của bạn. Bác sĩ sẽ kê toa một liều Avastin phù hợp với bạn. Bạn sẽ được điều trị bằng Avastin cứ sau 2 hoặc 3 tuần. Số lượng dịch truyền mà bạn nhận được sẽ phụ thuộc vào cách bạn đáp ứng với điều trị; bạn nên tiếp tục nhận thuốc này cho đến khi Avastin không thể ngăn chặn khối u phát triển. Bác sĩ sẽ thảo luận điều này với bạn.
Phương pháp và lộ trình quản trị
Avastin là giải pháp truyền dịch. Tùy thuộc vào liều lượng quy định cho bạn, một số hoặc tất cả nội dung của lọ Avastin sẽ được pha loãng với dung dịch natri clorua trước khi sử dụng. Một bác sĩ hoặc y tá sẽ cung cấp cho bạn dung dịch Avastin pha loãng này bằng cách truyền tĩnh mạch (nhỏ giọt vào tĩnh mạch của bạn). Truyền dịch đầu tiên sẽ được trao cho bạn trong hơn 90 phút. Nếu điều này được dung nạp tốt, truyền dịch thứ hai có thể được đưa ra trong hơn 60 phút. Truyền dịch sau này có thể được trao cho bạn trong hơn 30 phút.
Chú ý đề phòng và thận trọng
Vui lòng tham khảo ý kiến bác sĩ của bạn, ngay cả khi những tuyên bố trên chỉ áp dụng cho bạn trong quá khứ.
Trước khi bạn được cung cấp Avastin hoặc trong khi bạn đang được điều trị bằng Avastin:
- nếu bạn có hoặc bị đau miệng, răng và / hoặc hàm, sưng hoặc lở loét trong miệng, tê hoặc cảm giác nặng ở hàm, hoặc nới lỏng răng hãy báo cho bác sĩ và nha sĩ ngay lập tức.
- nếu bạn cần trải qua một điều trị nha khoa xâm lấn hoặc phẫu thuật nha khoa, hãy nói với nha sĩ của bạn rằng bạn đang được điều trị bằng Avastin, đặc biệt là khi bạn cũng đang nhận hoặc đã tiêm bisphosphonate vào máu.
Bạn có thể được khuyên nên kiểm tra răng miệng trước khi bắt đầu điều trị bằng Avastin.
Trẻ em và thanh thiếu niên
Sử dụng Avastin không được khuyến cáo ở trẻ em và thanh thiếu niên dưới 18 tuổi vì sự an toàn và lợi ích chưa được thiết lập trong các quần thể bệnh nhân này.
Cái chết của mô xương (hoại tử xương) trong xương khác với hàm đã được báo cáo ở những bệnh nhân dưới 18 tuổi khi điều trị bằng Avastin.
Mang thai, cho con bú và khả năng sinh sản
Bạn không được sử dụng thuốc này nếu bạn đang mang thai. Avastin có thể gây ra thiệt hại cho thai nhi của bạn vì nó có thể ngăn chặn sự hình thành các mạch máu mới. Bác sĩ nên tư vấn cho bạn về việc sử dụng biện pháp tránh thai trong khi điều trị bằng Avastin và trong ít nhất 6 tháng sau liều Avastin cuối cùng.
Hãy nói thẳng với bác sĩ nếu bạn đang mang thai, mang thai trong khi điều trị bằng thuốc này hoặc dự định có thai trong tương lai gần.
Bạn không được cho con bú trong khi điều trị bằng Avastin và trong ít nhất 6 tháng sau liều Avastin cuối cùng, vì thuốc này có thể cản trở sự tăng trưởng và phát triển của bé.
Avastin có thể làm giảm khả năng sinh sản của nữ giới. Vui lòng tham khảo ý kiến bác sĩ để biết thêm thông tin.
Hãy hỏi bác sĩ, dược sĩ hoặc y tá để được tư vấn trước khi dùng bất kỳ loại thuốc nào.
Lái xe và sử dụng máy móc
Avastin chưa được chứng minh là làm giảm khả năng lái xe hoặc sử dụng bất kỳ công cụ hoặc máy móc nào. Tuy nhiên, buồn ngủ và ngất đã được báo cáo khi sử dụng Avastin. Nếu bạn gặp các triệu chứng ảnh hưởng đến thị lực hoặc sự tập trung hoặc khả năng phản ứng của bạn, đừng lái xe và sử dụng máy cho đến khi các triệu chứng biến mất.
Tương tác thuốc
Hãy cho bác sĩ, dược sĩ hoặc y tá của bạn nếu bạn đang dùng, gần đây đã uống hoặc có thể dùng bất kỳ loại thuốc nào khác.
Sự kết hợp của Avastin với một loại thuốc khác gọi là sunitinib malate (được kê toa cho ung thư thận và đường tiêu hóa) có thể gây ra tác dụng phụ nghiêm trọng. Thảo luận với bác sĩ của bạn để đảm bảo rằng bạn không kết hợp các loại thuốc này.
Hãy cho bác sĩ của bạn nếu bạn đang sử dụng các liệu pháp dựa trên bạch kim hoặc taxane cho ung thư vú di căn hoặc phổi. Những liệu pháp này kết hợp với Avastin có thể làm tăng nguy cơ tác dụng phụ nghiêm trọng.
Xin vui lòng cho bác sĩ của bạn nếu bạn đã nhận được gần đây, hoặc đang nhận được, xạ trị.
Tác dụng không mong muốn
- Avastin có thể làm tăng nguy cơ phát triển các lỗ trên thành ruột. Nếu bạn có tình trạng gây viêm bên trong bụng (ví dụ viêm túi thừa, loét dạ dày, viêm đại tràng liên quan đến hóa trị liệu), vui lòng thảo luận với bác sĩ của bạn.
- Avastin có thể làm tăng nguy cơ phát triển một kết nối bất thường hoặc lối đi giữa hai cơ quan. Nguy cơ phát triển các kết nối giữa âm đạo và bất kỳ bộ phận nào của ruột có thể tăng lên nếu bạn bị ung thư cổ tử cung dai dẳng, tái phát hoặc di căn.
- Thuốc này có thể làm tăng nguy cơ chảy máu hoặc tăng nguy cơ các vấn đề với việc chữa lành vết thương sau phẫu thuật. Nếu bạn chuẩn bị phẫu thuật, nếu bạn đã có một cuộc phẫu thuật lớn trong vòng 28 ngày qua hoặc nếu bạn vẫn còn một vết thương chưa lành sau phẫu thuật, bạn không nên dùng thuốc này.
- Avastin có thể làm tăng nguy cơ phát triển nhiễm trùng nghiêm trọng của da hoặc các lớp sâu hơn dưới da, đặc biệt là nếu bạn có lỗ hổng trên thành ruột hoặc các vấn đề với việc chữa lành vết thương.
- Avastin có thể làm tăng tỷ lệ mắc bệnh cao huyết áp. Nếu bạn bị huyết áp cao mà không được kiểm soát tốt bằng thuốc huyết áp, vui lòng tham khảo ý kiến bác sĩ vì điều quan trọng là phải đảm bảo rằng huyết áp của bạn được kiểm soát trước khi bắt đầu điều trị Avastin.
- Nếu bạn đã hoặc đã bị phình động mạch (mở rộng và suy yếu thành mạch máu) hoặc rách trong thành mạch máu.
- Thuốc này làm tăng nguy cơ có protein trong nước tiểu của bạn đặc biệt là nếu bạn đã bị huyết áp cao.
- Nguy cơ phát triển cục máu đông trong động mạch của bạn (một loại mạch máu) có thể tăng nếu bạn trên 65 tuổi, nếu bạn bị tiểu đường, hoặc nếu bạn đã có cục máu đông trước đó trong động mạch. Hãy nói chuyện với bác sĩ của bạn vì cục máu đông có thể dẫn đến đau tim và đột quỵ.
- Avastin cũng có thể làm tăng nguy cơ hình thành cục máu đông trong tĩnh mạch của bạn (một loại mạch máu).
- Thuốc này có thể gây chảy máu, đặc biệt là chảy máu liên quan đến khối u. Vui lòng tham khảo ý kiến bác sĩ nếu bạn hoặc gia đình của bạn có xu hướng bị các vấn đề chảy máu hoặc bạn đang dùng thuốc để làm loãng máu vì bất kỳ lý do nào.
- Avastin có thể gây chảy máu trong và xung quanh não của bạn. Vui lòng thảo luận với bác sĩ của bạn nếu bạn bị ung thư di căn ảnh hưởng đến não của bạn.
- Có thể Avastin có thể làm tăng nguy cơ chảy máu trong phổi của bạn, bao gồm ho hoặc khạc ra máu. Vui lòng thảo luận với bác sĩ của bạn nếu bạn nhận thấy điều này trước đây.
- Avastin có thể làm tăng nguy cơ phát triển một trái tim yếu. Điều quan trọng là bác sĩ của bạn biết nếu bạn đã từng sử dụng anthracycline (ví dụ doxorubicin, một loại hóa trị cụ thể được sử dụng để điều trị một số bệnh ung thư) hoặc xạ trị ở ngực hoặc nếu bạn bị bệnh tim.
- Thuốc này có thể gây nhiễm trùng và giảm số lượng bạch cầu trung tính của bạn (một loại tế bào máu quan trọng để bảo vệ bạn chống lại vi khuẩn).
- Có thể Avastin có thể gây ra phản ứng quá mẫn và / hoặc truyền dịch (các phản ứng liên quan đến việc bạn tiêm thuốc). Xin vui lòng cho bác sĩ, dược sĩ hoặc y tá của bạn biết nếu trước đó bạn đã gặp vấn đề sau khi tiêm, chẳng hạn như chóng mặt / cảm giác ngất, khó thở, sưng hoặc phát ban da.
- Một tác dụng phụ thần kinh hiếm gặp có tên là hội chứng não có thể đảo ngược sau (PRES) có liên quan đến điều trị Avastin. Nếu bạn bị đau đầu, thay đổi thị lực, nhầm lẫn hoặc co giật có hoặc không có huyết áp cao, vui lòng liên hệ với bác sĩ của bạn.
Bạn nên tìm kiếm sự giúp đỡ ngay lập tức nếu bạn gặp phải bất kỳ tác dụng phụ nào được đề cập dưới đây.
Các tác dụng phụ nghiêm trọng
Có thể rất phổ biến (ảnh hưởng đến hơn 1 người dùng trong 10), bao gồm:
- huyết áp cao,
- cảm giác tê hoặc ngứa ran ở tay hoặc chân,
- giảm số lượng tế bào trong máu, bao gồm các tế bào trắng giúp chống lại nhiễm trùng (điều này có thể đi kèm với sốt) và các tế bào giúp máu đóng cục,
- cảm thấy yếu đuối và không có năng lượng,
- mệt mỏi,
- tiêu chảy, buồn nôn, nôn và đau bụng.
Các tác dụng phụ nghiêm trọng
Có thể phổ biến (ảnh hưởng đến 1 đến 10 người dùng trong 100), bao gồm:
- thủng ruột,
- chảy máu, bao gồm chảy máu ở phổi ở bệnh nhân ung thư phổi không phải tế bào nhỏ,
- chặn các động mạch bằng cục máu đông,
- chặn các tĩnh mạch bởi một cục máu đông,
- chặn các mạch máu của phổi bằng cục máu đông,
- chặn các tĩnh mạch chân bằng cục máu đông,
- suy tim
- vấn đề chữa lành vết thương sau phẫu thuật,
- đỏ, bong tróc, đau, đau hoặc phồng rộp trên ngón tay hoặc bàn chân,
- giảm số lượng hồng cầu trong máu,
- thiếu năng lượng,
- rối loạn dạ dày và ruột,
- đau cơ và khớp, yếu cơ,
- khô miệng kết hợp với khát và / hoặc nước tiểu giảm hoặc sẫm màu,
- viêm niêm mạc miệng ẩm và ruột, phổi và đường dẫn khí, đường sinh sản và đường tiết niệu,
- vết loét trong miệng và ống từ miệng đến dạ dày, có thể gây đau và gây khó nuốt,
- đau, bao gồm đau đầu, đau lưng và đau ở vùng xương chậu và hậu môn,
- bộ sưu tập mủ cục bộ,
- nhiễm trùng, và đặc biệt là nhiễm trùng trong máu hoặc bàng quang,
- giảm cung cấp máu cho não hoặc đột quỵ,
- buồn ngủ,
- chảy máu mũi,
- tăng nhịp tim (mạch),
- tắc nghẽn trong ruột hoặc ruột,
- xét nghiệm nước tiểu bất thường (protein trong nước tiểu),
- Khó thở hoặc nồng độ oxy trong máu thấp,
- nhiễm trùng da hoặc các lớp sâu hơn dưới da,
- lỗ rò: kết nối giống như ống bất thường giữa các cơ quan nội tạng và da hoặc các mô khác thường không được kết nối, bao gồm cả kết nối giữa âm đạo và ruột ở bệnh nhân ung thư cổ tử cung.
Quá liều
Nếu dùng quá nhiều Avastin
- Bạn có thể bị đau nửa đầu nghiêm trọng Nếu điều này xảy ra, bạn nên nói chuyện với bác sĩ, dược sĩ hoặc y tá ngay lập tức.
Bảo quản
Lọ (chưa mở) hạn sử dụng 2 năm.
Dược phẩm pha loãng
Độ ổn định sử dụng hóa học và vật lý đã được chứng minh trong 48 giờ ở 2 ° C đến 30 ° C trong dung dịch natri clorua 9 mg / ml (0,9%) khi tiêm. Từ quan điểm vi sinh, sản phẩm nên được sử dụng ngay lập tức. Nếu không được sử dụng ngay lập tức, thời gian và điều kiện lưu trữ sử dụng là trách nhiệm của người dùng và thông thường sẽ không dài hơn 24 giờ ở 2 ° C đến 8 ° C, trừ khi việc pha loãng đã diễn ra trong điều kiện vô trùng được kiểm soát và xác nhận.
Lưu trữ trong tủ lạnh (2 ° C-8 ° C).
Không đóng băng.
Giữ lọ trong thùng carton bên ngoài để tránh ánh sáng.
Dược lực học của thuốc Avastin
Cơ chế tác dụng của thuốc Avastin
Bevacizumab liên kết với yếu tố tăng trưởng nội mô mạch máu (VEGF), yếu tố chính thúc đẩy sự phát sinh mạch máu và sự hình thành mạch, và do đó ức chế sự gắn kết của VEGF với các thụ thể của nó, Flt-1 (VEGFR-1) và KDR (VEGFR-2) trên bề mặt tế bào nội mô. Trung hòa hoạt động sinh học của VEGF làm thoái hóa các khối u, bình thường hóa mạch máu khối u còn lại và ức chế sự hình thành mạch máu khối u mới, do đó ức chế sự phát triển của khối u.
Dược lực học thuốc Avastin
Sử dụng bevacizumab hoặc kháng thể murine của cha mẹ đối với các mô hình ung thư xenotransplant ở chuột nude dẫn đến hoạt động chống khối u rộng rãi trong ung thư ở người, bao gồm đại tràng, vú, tuyến tụy và tuyến tiền liệt. Tiến triển bệnh di căn bị ức chế và tính thấm của vi mạch đã giảm.
Dược động học của thuốc Avastin
Dược động học của thuốc Avastin với đối tượng chung
Dữ liệu dược động học của bevacizumab có sẵn từ mười thử nghiệm lâm sàng ở bệnh nhân có khối u rắn. Trong tất cả các thử nghiệm lâm sàng, bevacizumab được dùng dưới dạng tiêm truyền IV. Tốc độ truyền dịch dựa trên khả năng dung nạp, với thời gian truyền ban đầu là 90 phút. Dược động học của bevacizumab là tuyến tính với liều từ 1 đến 10 mg / kg.
Phân bố
Giá trị điển hình cho thể tích trung tâm (V c ) là 2,73 L và 3,28 L đối với bệnh nhân nữ và nam tương ứng, nằm trong phạm vi đã được mô tả cho IgGs và các kháng thể đơn dòng khác. Giá trị điển hình cho thể tích ngoại vi (V p ) lần lượt là 1,69 L và 2,35 L đối với bệnh nhân nữ và nam, khi bevacizumab được dùng chung với các thuốc chống tân sinh. Sau khi điều chỉnh trọng lượng cơ thể, bệnh nhân nam có V c (+ 20%) lớn hơn bệnh nhân nữ.
Biến đổi sinh học
Đánh giá sự trao đổi chất bevacizumab ở thỏ sau một liều IV 125 I-bevacizumab chỉ ra rằng hồ sơ trao đổi chất của nó tương tự như dự kiến đối với phân tử IgG tự nhiên không gắn VEGF. Sự chuyển hóa và đào thải bevacizumab tương tự như IgG nội sinh, chủ yếu thông qua quá trình dị hóa protein trên toàn cơ thể, bao gồm các tế bào nội mô và không phụ thuộc chủ yếu vào việc đào thải qua thận và gan. Liên kết IgG với thụ thể FcRn dẫn đến sự bảo vệ khỏi sự trao đổi chất của tế bào và thời gian bán hủy cuối cùng dài.
Thải trừ
Giá trị giải phóng mặt bằng, trung bình, bằng 0,188 và 0,220 L / ngày đối với bệnh nhân nữ và nam, tương ứng. Sau khi điều chỉnh trọng lượng cơ thể, bệnh nhân nam có độ thanh thải bevacizumab cao hơn (+ 17%) so với nữ giới. Theo mô hình hai ngăn, thời gian bán hủy là 18 ngày đối với một bệnh nhân nữ điển hình và 20 ngày đối với một bệnh nhân nam điển hình.
Albumin thấp và gánh nặng khối u cao thường là dấu hiệu của mức độ nghiêm trọng của bệnh. Độ thanh thải Bevacizumab nhanh hơn khoảng 30% ở những bệnh nhân có nồng độ albumin huyết thanh thấp và nhanh hơn 7% ở những người có gánh nặng khối u cao hơn khi so sánh với một bệnh nhân điển hình có giá trị trung bình của albumin và gánh nặng khối u.
Dược động học trong quần thể đặc biệt
Dược động học dân số được phân tích ở bệnh nhân người lớn và trẻ em để đánh giá ảnh hưởng của các đặc điểm nhân khẩu học. Ở người lớn, kết quả cho thấy không có sự khác biệt đáng kể về dược động học của bevacizumab so với tuổi.
Suy thận
Không có thử nghiệm nào được thực hiện để điều tra dược động học của bevacizumab ở bệnh nhân suy thận vì thận không phải là cơ quan chính để chuyển hóa hoặc bài tiết bevacizumab.
Suy gan
Không có thử nghiệm nào được thực hiện để điều tra dược động học của bevacizumab ở bệnh nhân suy gan vì gan không phải là cơ quan chính để chuyển hóa hoặc bài tiết bevacizumab.
Trẻ em
Dược động học của bevacizumab được đánh giá ở 152 trẻ em, thanh thiếu niên và thanh niên (7 tháng đến 21 tuổi, 5,9 đến 125 kg) qua 4 nghiên cứu lâm sàng sử dụng mô hình dược động học dân số. Kết quả dược động học cho thấy độ thanh thải và thể tích phân phối của bevacizumab tương đương giữa bệnh nhân trẻ em và người trưởng thành trẻ tuổi khi bình thường hóa trọng lượng cơ thể, với xu hướng tiếp xúc thấp hơn khi trọng lượng cơ thể giảm. Tuổi không liên quan đến dược động học của bevacizumab khi trọng lượng cơ thể được tính đến.
Dược động học của bevacizumab được đặc trưng bởi mô hình PK dân số nhi khoa cho 70 bệnh nhân trong nghiên cứu BO20924 ((1,4 đến 17,6 năm; 11,6 đến 77,5 kg) và 59 bệnh nhân trong nghiên cứu BO25041 (1 đến 17 tuổi; 11,2 đến 82,3 kg). Nghiên cứu BO20924, phơi nhiễm bevacizumab thường thấp hơn so với một bệnh nhân trưởng thành điển hình ở cùng liều. Trong nghiên cứu BO25041, phơi nhiễm bevacizumab tương tự như một người trưởng thành điển hình ở cùng liều. Trong cả hai nghiên cứu, phơi nhiễm bevacizumb có xu hướng giảm khi trọng lượng cơ thể giảm.